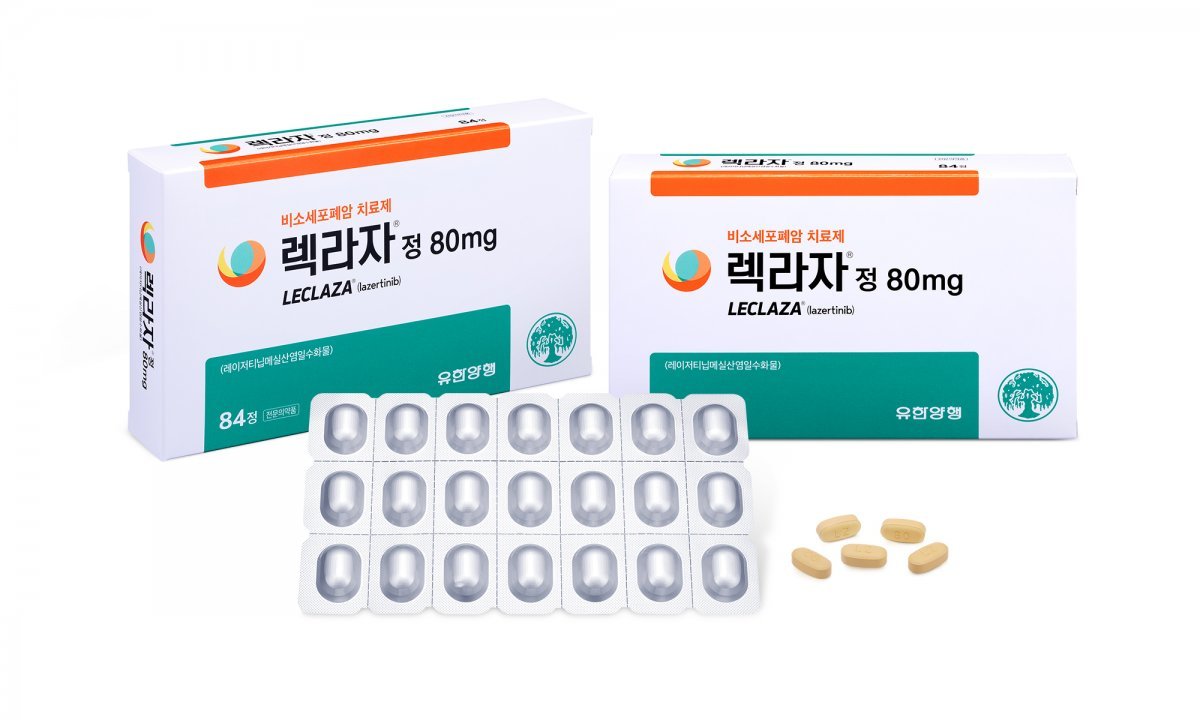
유한양행은 폐암 신약 렉라자가 식품의약품안전처(이하 식약처)로부터 상피세포 성장인자 수용체(EGFR) 돌연변이 양성 비소세포폐암(NSCLC)의 1차 치료제로 허가받았다고 6월30일 공시했다.
렉라자는 2021년 1월 18일 식약처로부터 EGFR T790M 돌연변이 양성 2차 치료제로 허가 받은 제품이다. 지난해 10월 다국가 임상 3상 시험에서 통계적으로 의미있는 무진행 생존기간(PFS) 개선을 확인한 뒤 올해 3월에 EGFR 변이 양성 1차 치료제로 국내 품목 허가 신청서를 제출하였다.
김열홍 유한양행 R&D 총괄 사장은, “유한양행의 과학적 역량과 끊임없는 노력으로 탄생한 약제로 이번 허가로 국내에서 유병률이 높은 EGFR 변이 양성 비소세포폐암 환자들에게 새로운 치료 옵션을 제공할 수 있어 매우 기쁘다”고 밝혔다.
현재 유한양행은 1차 치료제로 렉라자 급여 기준 확대 신청을 준비하고 있으며 건강보험 급여 처방 가능 시점까지 환자들에게 무상으로 약제를 제공하는 인도적 차원의 프로그램(EAP)을 준비하고 있다. 해당 프로그램은 각 기관생명윤리위원회(IRB) 승인일로부터 렉라자의 급여 기준 확대 시점까지 진행할 예정이다.
스포츠동아 김재범 기자 oldfield@donga.com
Copyright © 스포츠동아. All rights reserved. 무단 전재, 재배포 및 AI학습 이용 금지
공유하기







![옥주현, 과감+강렬한 수영복 뒤태 [DA★]](https://dimg.donga.com/a/158/89/95/1/wps/SPORTS/IMAGE/2023/07/01/120029759.1.jpg)







![이주연, 9년 전 안 믿겨…누드톤 각선미+무결점 바디라인 [DA★]](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133473742.1.jpg)
![[단독] 히말라야 편성 갈등? jtbc “우리와 무관한 행사”](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133472616.1.jpg)


![기안84, ‘기안장2’ 스태프 150명 사비 선물…미담 터졌다 [SD톡톡]](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133471769.1.png)


![이시안 수위 조절 실패…코 성형 구축설+김고은 겹지인 고백 [DA클립]](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133471521.1.jpg)



![‘구독자 100만 임박’ 김선태, 영향력 어디까지…사칭 계정 등장 [DA이슈]](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133471314.3.jpg)
![“콧구멍 변해” 백지영, 성형 10억설 고백…정석원 ‘연골 약속♥’ [DA클립]](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133472619.1.jpg)
![‘1세대 톱모델’ 홍진경·이소라, 파리서 ‘본업 모먼트’ 포착 [DA★]](https://dimg.donga.com/a/232/174/95/1/wps/SPORTS/IMAGE/2026/03/05/133471351.1.jpg)


![캐나다 行 ‘이휘재♥’ 문정원, 4년 만 근황…“어느새 3월” [DA이슈]](https://dimg.donga.com/a/72/72/95/1/wps/SPORTS/IMAGE/2026/03/04/133459538.1.jpg)
![문가영, 어깨라인 드러낸 오프숄더…청초 비주얼 [DA★]](https://dimg.donga.com/a/72/72/95/1/wps/SPORTS/IMAGE/2026/03/03/133452786.1.jpg)

![샤라포바, 이탈리아서 뽐낸 수영복 자태…몸매 여전해 [DA★]](https://dimg.donga.com/a/72/72/95/1/wps/SPORTS/IMAGE/2026/03/03/133452477.1.jpg)
![장희진, 청순 미모에 그렇지 못한 몸매…애플힙까지 ‘완벽’ [DA★]](https://dimg.donga.com/a/140/140/95/1/wps/SPORTS/IMAGE/2026/03/05/133474200.1.jpg)
![‘환승연애4’ 박현지 민낯도 완벽한데 “얼굴 보고 ‘현타’” [DA클립]](https://dimg.donga.com/a/140/140/95/1/wps/SPORTS/IMAGE/2026/03/05/133474117.1.jpg)
![김연경 “이상형=일편단심 조인성♥, 몇 번 만나” 어머 세상에 [DA클립]](https://dimg.donga.com/a/140/140/95/1/wps/SPORTS/IMAGE/2026/03/05/133474072.1.jpg)



![“미쳤나”…로버트 할리, 아내에 물 뿌렸다 ‘충격 고백’ [DA클립]](https://dimg.donga.com/a/72/72/95/1/wps/SPORTS/IMAGE/2026/03/05/133467406.1.jpg)















![장예원 주식 대박 터졌다, 수익률 무려 323.53% [DA★]](https://dimg.donga.com/a/110/73/95/1/wps/SPORTS/IMAGE/2023/12/01/122442320.1.jpg)







댓글 0